Białka z rodziny IAP (z ang. inhibitors of apoptosis)
Rodzina białek komórkowych zaangażowanych w regulację apoptozy komórki. IAP to białka hamujące transdukcję sygnału śmierci w komórce. Mechanizm ich oddziaływania polega na tworzeniu kompleksów z innymi białkami uczestniczącymi w transdukcji apoptozy. Hamowaniu podlegają głównie kaspazy ale także białka adapterowe, czynniki transkrypcyjne, lub ich blokery. Białka IAP mogą hamować zatem zarówno szlak zewnątrz- jak i wewnątrzpochodny apoptozy. U ssaków zidentyfikowano dotychczas kilka białek rodziny IAP, m.in.: XIAP, cIAP2, NAIP, liwinę i surwiwinę.
Białka IAP są zabudowane z łańcucha o długości od 150 do 1500 aminokwasów, których cechą charakterystyczną jest obecność dwóch motywów sekwencyjnych – domeny BIR (baculoviral IAP-like repeats) oraz domeny RING (really interesting new gene). Domena RING ma aktywność liagzy i jest zlokalizowana w C-końcu białka. Białka IAP różnią się między sobą liczbą domen zawartych w sekwencji polipeptydowej. W sekwencji polipeptydu białka XIAP są zawarte trzy domeny BIR, wśród których domena BIR-2 odpowiada za hamowanie kaspazy 3 i 7 oraz pośredniczy w oddziaływaniu z białkiem Smac/DIABLO. BIR3 z kolei wchodzi z interakcję z kaspazą 9, blokując jej aktywację. Schematyczna ilustracja struktury polipeptydów białek IAP jest przedstawiona na rysunku 1.
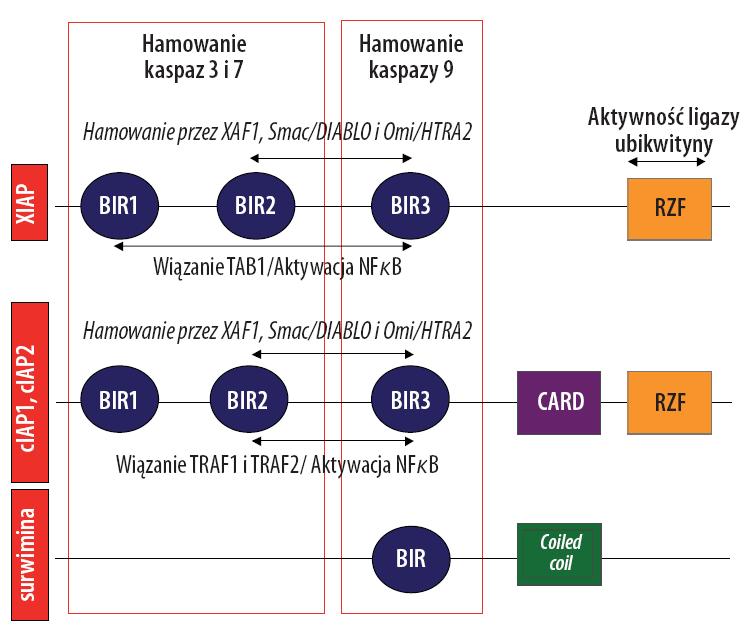
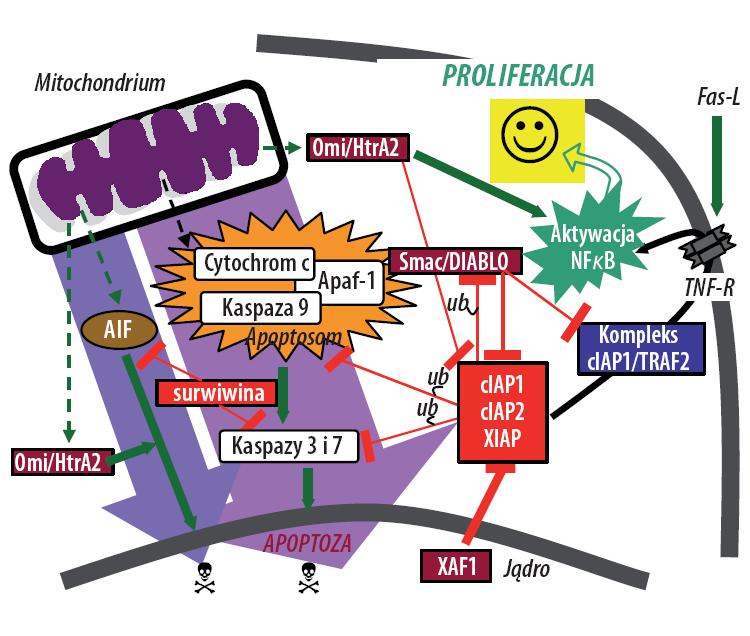
Większość IAP ma zdolność bezpośredniego unieczynnienia kaspaz wykonawczych (3 i 7) oraz zapobiega aktywacji kaspazy 9, będącej inicjatorem szlaku mitochondrialnego apoptozy. IAP mogą działać także jako ligazy, przyczyniając się do degradacji kaspaz. Badania wskazują także na dodatkową możliwość oddziaływania białek cIAP1 i cIAP2 z elementami sygnalosomów receptorów błonowych, białkami TRAF1 i TRAF2, hamując inicjację drogi zewnątrzpochodnej. Badania ostatnich lat wykazały, że w komórkach są obecne także antagoniści działania IAP. Znane są obecnie trzy białka, które po uwolnieniu z mitochondriom wiążą się z XIAP, cIAP1, cIAP2 i surwiwiną. Do białek tych należą między innymi: Smac/DIABLO i HtrA2/Omi. Schematyczna ilustracja transdukcji dróg apoptozy z zaznaczeniem roli białek IAP jest przedstawiona na rysunku 2.
Piśmiennictwo: